În domeniul medicinei moderne, antibioticele s-au dovedit a fi unul dintre cele mai semnificative progrese, reducând dramatic incidența și ratele de mortalitate asociate cu infecțiile microbiene. Capacitatea lor de a modifica rezultatele clinice ale infecțiilor bacteriene a prelungit speranța de viață a nenumărați pacienți. Antibioticele sunt esențiale în procedurile medicale complexe, inclusiv intervenții chirurgicale, plasarea de implanturi, transplanturi și chimioterapie. Cu toate acestea, apariția agenților patogeni rezistenți la antibiotice a reprezentat o preocupare tot mai mare, diminuând eficacitatea acestor medicamente în timp. Au fost documentate cazuri de rezistență la antibiotice în toate categoriile de antibiotice, pe măsură ce apar mutații microbiene. Presiunea de selecție exercitată de medicamentele antimicrobiene a contribuit la creșterea tulpinilor rezistente, reprezentând o provocare semnificativă pentru sănătatea globală.
Pentru a combate problema presantă a rezistenței antimicrobiene, este esențial să se implementeze politici eficiente de control al infecțiilor care să reducă răspândirea agenților patogeni rezistenți, reducând totodată utilizarea antibioticelor. În plus, există o nevoie stringentă de metode alternative de tratament. Terapia cu oxigen hiperbaric (HBOT) a apărut ca o modalitate promițătoare în acest context, implicând inhalarea de oxigen 100% la anumite niveluri de presiune pentru o perioadă de timp. Poziționată fie ca tratament primar, fie complementar pentru infecții, HBOT poate oferi o nouă speranță în tratarea infecțiilor acute cauzate de agenți patogeni rezistenți la antibiotice.
Această terapie este aplicată din ce în ce mai mult ca tratament primar sau alternativ pentru diverse afecțiuni, inclusiv inflamații, intoxicații cu monoxid de carbon, plăgi cronice, boli ischemice și infecții. Aplicațiile clinice ale HBOT în tratamentul infecțiilor sunt profunde, oferind avantaje neprețuite pacienților.

Aplicații clinice ale terapiei cu oxigen hiperbaric în infecții
Dovezile actuale susțin în mod solid aplicarea HBOT, atât ca tratament independent, cât și adjuvant, prezentând beneficii semnificative pentru pacienții infectați. În timpul HBOT, tensiunea arterială a oxigenului din sânge poate crește până la 2000 mmHg, iar gradientul ridicat de presiune oxigen-țesut rezultat poate ridica nivelurile de oxigen tisular la 500 mmHg. Astfel de efecte sunt deosebit de valoroase în promovarea vindecării răspunsurilor inflamatorii și a perturbărilor microcirculatorii observate în mediile ischemice, precum și în gestionarea sindromului de compartiment.
HBOT poate influența, de asemenea, afecțiunile care depind de sistemul imunitar. Cercetările indică faptul că HBOT poate suprima sindroamele autoimune și răspunsurile imune induse de antigen, contribuind la menținerea toleranței la grefă prin reducerea circulației limfocitelor și leucocitelor, modulând în același timp răspunsurile imune. În plus, HBOTsusține vindecareaîn leziunile cronice ale pielii prin stimularea angiogenezei, un proces esențial pentru o recuperare îmbunătățită. Această terapie încurajează, de asemenea, formarea matricei de colagen, o fază esențială în vindecarea rănilor.
O atenție specială trebuie acordată anumitor infecții, în special infecțiilor profunde și dificil de tratat, cum ar fi fasciita necrozantă, osteomielita, infecțiile cronice ale țesuturilor moi și endocardita infecțioasă. Una dintre cele mai frecvente aplicații clinice ale HBOT este pentru infecțiile pielii și țesuturilor moi și osteomielita asociată cu niveluri scăzute de oxigen, care sunt adesea cauzate de bacterii anaerobe sau rezistente.
1. Infecții ale piciorului diabetic
Piciorul diabeticUlcerele sunt o complicație prevalentă în rândul pacienților diabetici, afectând până la 25% din această populație. Infecțiile apar frecvent în aceste ulcere (reprezentând 40%-80% din cazuri) și duc la o creștere a morbidității și mortalității. Infecțiile piciorului diabetic (IFD) constau de obicei în infecții polimicrobiene cu o varietate de agenți patogeni bacterieni anaerobi identificați. Diverși factori, inclusiv defectele funcției fibroblastelor, problemele de formare a colagenului, mecanismele imune celulare și funcția fagocitelor, pot împiedica vindecarea rănilor la pacienții diabetici. Mai multe studii au identificat oxigenarea deficitară a pielii ca un factor de risc puternic pentru amputările legate de IDF.
Ca una dintre opțiunile actuale pentru tratamentul DFIS-a raportat că HBOT îmbunătățește semnificativ ratele de vindecare a ulcerelor piciorului diabetic, reducând ulterior necesitatea amputărilor și a intervențiilor chirurgicale complicate. Nu numai că minimizează necesitatea procedurilor care necesită multe resurse, cum ar fi intervențiile chirurgicale cu lambou și grefa de piele, dar prezintă și costuri mai mici și efecte secundare minime în comparație cu opțiunile chirurgicale. Un studiu realizat de Chen și colab. a demonstrat că mai mult de 10 ședințe de HBOT au dus la o îmbunătățire cu 78,3% a ratelor de vindecare a rănilor la pacienții diabetici.
2. Infecții necrozante ale țesuturilor moi
Infecțiile necrozante ale țesuturilor moi (NSTI) sunt adesea polimicrobiene, de obicei provenind dintr-o combinație de agenți patogeni bacterieni aerobi și anaerobi și sunt adesea asociate cu producerea de gaze. Deși NSTI sunt relativ rare, acestea prezintă o rată ridicată a mortalității din cauza progresiei lor rapide. Diagnosticul și tratamentul la timp și adecvat sunt esențiale pentru obținerea unor rezultate favorabile, iar HBOT a fost recomandat ca metodă adjuvantă pentru gestionarea NSTI-urilor. Deși există încă controverse cu privire la utilizarea HBOT în NSTI-uri din cauza lipsei studiilor controlate prospective,Dovezile sugerează că ar putea fi corelat cu rate de supraviețuire îmbunătățite și conservarea organelor la pacienții cu ISTUn studiu retrospectiv a indicat o reducere semnificativă a ratelor mortalității în rândul pacienților cu infecții cutanate non-infectate care primesc HBOT.
1.3 Infecții ale locului chirurgical
Sindroamele infecțioase ale site-ului (SSI) pot fi clasificate în funcție de locul anatomic al infecției și pot apărea din cauza diverșilor agenți patogeni, inclusiv bacterii aerobe și anaerobe. În ciuda progreselor în măsurile de control al infecțiilor, cum ar fi tehnicile de sterilizare, utilizarea antibioticelor profilactice și îmbunătățirile practicilor chirurgicale, SSI rămân o complicație persistentă.
O analiză semnificativă a investigat eficacitatea HBOT în prevenirea infecțiilor sismice profunde în chirurgia scoliozei neuromusculare. HBOT preoperatorie poate reduce semnificativ incidența infecțiilor sismice și poate facilita vindecarea rănilor. Această terapie neinvazivă creează un mediu în care nivelurile de oxigen din țesuturile plăgii sunt ridicate, ceea ce a fost asociat cu acțiunea oxidativă de ucidere împotriva agenților patogeni. În plus, abordează nivelurile scăzute de sânge și oxigen care contribuie la dezvoltarea infecțiilor sismice. Dincolo de alte strategii de control al infecțiilor, HBOT a fost recomandat în special pentru intervențiile chirurgicale curate și contaminate, cum ar fi procedurile colorectale.
1.4 Arsuri
Arsurile sunt leziuni cauzate de căldură extremă, curent electric, substanțe chimice sau radiații și pot prezenta rate ridicate de morbiditate și mortalitate. HBOT este benefic în tratarea arsurilor prin creșterea nivelului de oxigen din țesuturile deteriorate. Deși studiile pe animale și clinice prezintă rezultate mixte în ceea ce privește...Eficacitatea HBOT în tratamentul arsurilorUn studiu care a implicat 125 de pacienți cu arsuri a indicat că HBOT nu a avut un impact semnificativ asupra ratelor de mortalitate sau asupra numărului de intervenții chirurgicale efectuate, dar a redus timpul mediu de vindecare (19,7 zile comparativ cu 43,8 zile). Integrarea HBOT cu gestionarea completă a arsurilor ar putea controla eficient sepsisul la pacienții cu arsuri, ducând la timpi de vindecare mai scurți și la un necesar redus de lichide. Cu toate acestea, sunt necesare cercetări prospective suplimentare ample pentru a confirma rolul HBOT în gestionarea arsurilor extinse.
1.5 Osteomielită
Osteomielita este o infecție a oaselor sau a măduvei osoase, adesea cauzată de agenți patogeni bacterieni. Tratarea osteomielitei poate fi dificilă din cauza alimentării cu sânge relativ slabe a oaselor și a penetrării limitate a antibioticelor în măduvă. Osteomielita cronică este caracterizată de agenți patogeni persistenți, inflamație ușoară și formarea de țesut osos necrotic. Osteomielita refractară se referă la infecții osoase cronice care continuă sau recidivează în ciuda tratamentului adecvat.
S-a demonstrat că HBOT îmbunătățește semnificativ nivelurile de oxigen din țesuturile osoase infectate. Numeroase serii de cazuri și studii de cohortă indică faptul că HBOT îmbunătățește rezultatele clinice pentru pacienții cu osteomielită. Se pare că acționează prin diverse mecanisme, inclusiv stimularea activității metabolice, suprimarea agenților patogeni bacterieni, sporirea efectelor antibioticelor, minimizarea inflamației și promovarea vindecării.procese. După HBOT, 60% până la 85% dintre pacienții cu osteomielită cronică refractară prezintă semne de supresie a infecției.
1.6 Infecții fungice
La nivel global, peste trei milioane de persoane suferă de infecții fungice cronice sau invazive, ceea ce duce la peste 600.000 de decese anual. Rezultatele tratamentului pentru infecțiile fungice sunt adesea compromise din cauza unor factori precum statusul imunitar alterat, bolile subiacente și caracteristicile de virulență ale agenților patogeni. HBOT devine o opțiune terapeutică atractivă în infecțiile fungice severe datorită siguranței și naturii sale neinvazive. Studiile indică faptul că HBOT ar putea fi eficient împotriva agenților patogeni fungici precum Aspergillus și Mycobacterium tuberculosis.
TOHB promovează efectele antifungice prin inhibarea formării biofilmului de Aspergillus, cu o eficiență crescută observată la tulpinile cărora le lipsesc genele superoxid dismutazei (SOD). Condițiile hipoxice din timpul infecțiilor fungice prezintă provocări pentru administrarea medicamentelor antifungice, făcând ca nivelurile crescute de oxigen cauzate de TOHB să fie o intervenție potențial benefică, deși sunt necesare cercetări suplimentare.
Proprietățile antimicrobiene ale HBOT
Mediul hiperoxic creat de HBOT inițiază modificări fiziologice și biochimice care stimulează proprietățile antibacteriene, ceea ce o face o terapie adjuvantă eficientă pentru infecții. HBOT demonstrează efecte remarcabile împotriva bacteriilor aerobe și predominant anaerobe prin mecanisme precum activitatea bactericidă directă, amplificarea răspunsurilor imune și efectele sinergice cu agenți antimicrobieni specifici.
2.1 Efecte antibacteriene directe ale HBOT
Efectul antibacterian direct al HBOT este atribuit în mare măsură generării de specii reactive de oxigen (ROS), care includ anioni superoxid, peroxid de hidrogen, radicali hidroxil și ioni hidroxil - toți aceștia apar în timpul metabolismului celular.
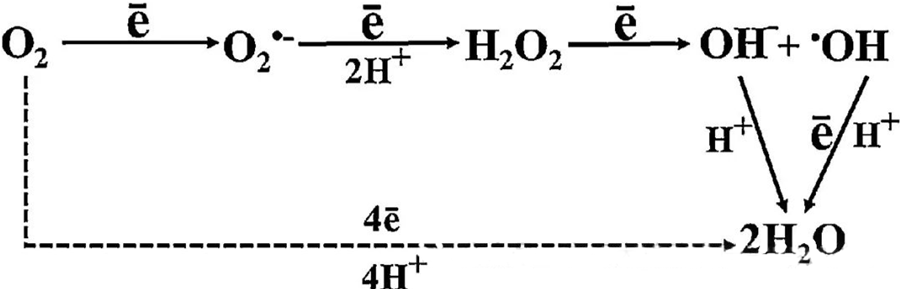
Interacțiunea dintre O₂ și componentele celulare este esențială pentru înțelegerea modului în care se formează ROS în celule. În anumite condiții denumite stres oxidativ, echilibrul dintre formarea ROS și degradarea acestora este perturbat, ceea ce duce la niveluri ridicate de ROS în celule. Producția de superoxid (O₂⁻) este catalizată de superoxid dismutaza, care ulterior transformă O₂⁻ în peroxid de hidrogen (H₂O₂). Această conversie este amplificată în continuare de reacția Fenton, care oxidează Fe²⁺ pentru a genera radicali hidroxil (·OH) și Fe³⁺, inițiind astfel o secvență redox dăunătoare de formare a ROS și deteriorare celulară.
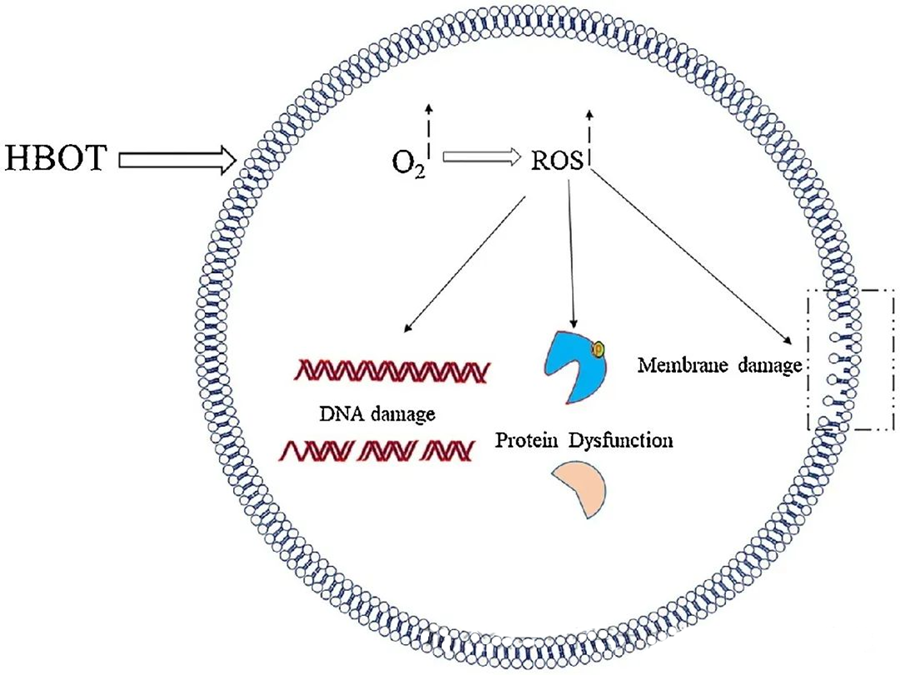
Efectele toxice ale ROS vizează componente celulare critice, cum ar fi ADN-ul, ARN-ul, proteinele și lipidele. În special, ADN-ul este o țintă principală a citotoxicității mediate de H₂O₂, deoarece perturbă structurile dezoxiribozei și deteriorează compozițiile bazice. Daunele fizice induse de ROS se extind la structura helix a ADN-ului, rezultând potențial din peroxidarea lipidică declanșată de ROS. Acest lucru subliniază consecințele negative ale nivelurilor ridicate de ROS în sistemele biologice.
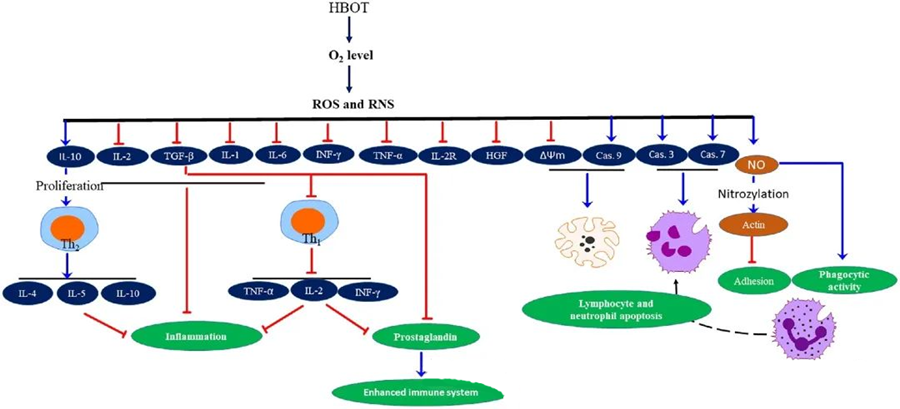
Acțiunea antimicrobiană a ROS
ROS joacă un rol vital în inhibarea creșterii microbiene, așa cum s-a demonstrat prin generarea de ROS indusă de HBOT. Efectele toxice ale ROS vizează direct constituenții celulari precum ADN-ul, proteinele și lipidele. Concentrațiile mari de specii de oxigen activ pot deteriora direct lipidele, ducând la peroxidarea lipidelor. Acest proces compromite integritatea membranelor celulare și, în consecință, funcționalitatea receptorilor și proteinelor asociate membranei.
În plus, proteinele, care sunt și ținte moleculare semnificative ale ROS, suferă modificări oxidative specifice la nivelul diferitelor reziduuri de aminoacizi, cum ar fi cisteina, metionina, tirozina, fenilalanina și triptofanul. De exemplu, s-a demonstrat că HBOT induce modificări oxidative în mai multe proteine din E. coli, inclusiv factorul de elongație G și DnaK, afectând astfel funcțiile lor celulare.
Îmbunătățirea imunității prin HBOT
Proprietățile antiinflamatorii ale HBOTau fost documentate, dovedindu-se cruciale pentru ameliorarea leziunilor tisulare și suprimarea progresiei infecției. HBOT are un impact semnificativ asupra expresiei citokinelor și a altor regulatori inflamatori, influențând răspunsul imun. Diverse sisteme experimentale au observat modificări diferențiale în expresia genelor și generarea de proteine post-HBOT, care fie suprareglează, fie subreglează factorii de creștere și citokinele.
În timpul procesului HBOT, nivelurile crescute de O₂ declanșează o serie de răspunsuri celulare, cum ar fi suprimarea eliberării mediatorilor proinflamatori și promovarea apoptozei limfocitelor și neutrofilelor. Împreună, aceste acțiuni sporesc mecanismele antimicrobiene ale sistemului imunitar, facilitând astfel vindecarea infecțiilor.
În plus, studiile sugerează că nivelurile crescute de O₂ în timpul HBOT pot reduce expresia citokinelor proinflamatorii, inclusiv interferon-gamma (IFN-γ), interleukina-1 (IL-1) și interleukina-6 (IL-6). Aceste modificări includ, de asemenea, reducerea raportului celulelor T CD4:CD8 și modularea altor receptori solubili, crescând în cele din urmă nivelurile de interleukină-10 (IL-10), ceea ce este crucial pentru contracararea inflamației și favorizarea vindecării.
Activitățile antimicrobiene ale HBOT sunt interconectate cu mecanisme biologice complexe. Atât superoxidul, cât și presiunea crescută au fost raportate ca promovând în mod inconsistent activitatea antibacteriană indusă de HBOT și apoptoza neutrofilelor. În urma HBOT, o creștere marcată a nivelului de oxigen sporește capacitățile bactericide ale neutrofilelor, o componentă esențială a răspunsului imun. În plus, HBOT suprimă aderența neutrofilelor, care este mediată de interacțiunea β-integrinelor de pe neutrofile cu moleculele de adeziune intercelulară (ICAM) de pe celulele endoteliale. HBOT inhibă activitatea integrinei β-2 a neutrofilelor (Mac-1, CD11b/CD18) printr-un proces mediat de oxid nitric (NO), contribuind la migrarea neutrofilelor către locul infecției.
Rearanjarea precisă a citoscheletului este necesară pentru ca neutrofilele să fagociteze eficient agenții patogeni. S-nitrozilarea actinei s-a dovedit a stimula polimerizarea actinei, facilitând potențial activitatea fagocitară a neutrofilelor după pretratamentul cu HBOT. Mai mult, HBOT promovează apoptoza în liniile de celule T umane prin căi mitocondriale, fiind raportată o moarte accelerată a limfocitelor post-HBOT. Blocarea caspazei-9 - fără a afecta caspaza-8 - a demonstrat efectele imunomodulatoare ale HBOT.
Efectele sinergice ale HBOT cu agenții antimicrobieni
În aplicațiile clinice, HBOT este frecvent utilizată alături de antibiotice pentru a combate eficient infecțiile. Starea hiperoxică obținută în timpul HBOT poate influența eficacitatea anumitor agenți antibiotici. Cercetările sugerează că anumite medicamente bactericide, cum ar fi β-lactamele, fluorochinolonele și aminoglicozidele, nu numai că acționează prin mecanisme inerente, ci se bazează parțial și pe metabolismul aerob al bacteriilor. Prin urmare, prezența oxigenului și caracteristicile metabolice ale agenților patogeni sunt esențiale atunci când se evaluează efectele terapeutice ale antibioticelor.
Dovezi semnificative au arătat că nivelurile scăzute de oxigen pot crește rezistența Pseudomonas aeruginosa la piperacilină/tazobactam și că un mediu cu conținut scăzut de oxigen contribuie, de asemenea, la creșterea rezistenței Enterobacter cloacae la azitromicină. În schimb, anumite condiții hipoxice pot crește sensibilitatea bacteriană la antibioticele tetracicline. HBOT servește ca o metodă terapeutică adjuvantă viabilă prin inducerea metabolismului aerob și reoxigenarea țesuturilor infectate hipoxic, crescând ulterior sensibilitatea agenților patogeni la antibiotice.
În studiile preclinice, combinația de HBOT – administrată de două ori pe zi timp de 8 ore la 280 kPa – alături de tobramicină (20 mg/kg/zi) a redus semnificativ încărcătura bacteriană în endocardita infecțioasă cu Staphylococcus aureus. Acest lucru demonstrează potențialul HBOT ca tratament auxiliar. Investigații ulterioare au arătat că, la 37°C și o presiune de 3 ATA timp de 5 ore, HBOT a sporit semnificativ efectele imipenemului împotriva Pseudomonas aeruginosa infectată cu macrofage. În plus, s-a constatat că modalitatea combinată de HBOT cu cefazolină este mai eficientă în tratarea osteomielitei cu Staphylococcus aureus la modelele animale, comparativ cu cefazolina administrată singură.
HBOT crește, de asemenea, semnificativ acțiunea bactericidă a ciprofloxacinei împotriva biofilmelor de Pseudomonas aeruginosa, în special după 90 de minute de expunere. Această creștere este atribuită formării speciilor reactive de oxigen (ROS) endogene și prezintă o sensibilitate sporită la mutanții cu deficit de peroxidază.
În modelele de pleurită cauzată de Staphylococcus aureus rezistent la meticilină (MRSA), efectul colaborativ al vancomicinei, teicoplaninei și linezolidului cu HBOT a demonstrat o eficacitate semnificativ crescută împotriva MRSA. Metronidazolul, un antibiotic utilizat pe scară largă în tratarea infecțiilor anaerobe și polimicrobiene severe, cum ar fi infecțiile piciorului diabetic (IFD) și infecțiile locului chirurgical (SSI), a demonstrat o eficacitate antimicrobiană mai mare în condiții anaerobe. Sunt necesare studii viitoare pentru a explora efectele antibacteriene sinergice ale HBOT combinat cu metronidazol, atât in vivo, cât și in vitro.
Eficacitatea antimicrobiană a HBOT asupra bacteriilor rezistente
Odată cu evoluția și răspândirea tulpinilor rezistente, antibioticele tradiționale își pierd adesea potența în timp. În plus, HBOT se poate dovedi esențial în tratarea și prevenirea infecțiilor cauzate de agenți patogeni multirezistenți la medicamente, servind ca o strategie critică atunci când tratamentele cu antibiotice eșuează. Numeroase studii au raportat efectele bactericide semnificative ale HBOT asupra bacteriilor rezistente relevante clinic. De exemplu, o sesiune HBOT de 90 de minute la 2 ATM a redus substanțial creșterea MRSA. În plus, în modelele de raport, HBOT a sporit efectele antibacteriene ale diferitelor antibiotice împotriva infecțiilor cu MRSA. Rapoartele au confirmat că HBOT este eficient în tratarea osteomielitei cauzate de Klebsiella pneumoniae producătoare de OXA-48, fără a fi necesară administrarea de antibiotice adjuvante.
În concluzie, terapia cu oxigen hiperbaric reprezintă o abordare multifațetată a controlului infecțiilor, sporind răspunsul imun și amplificând în același timp eficacitatea agenților antimicrobieni existenți. Cu cercetări și dezvoltări ample, aceasta are potențialul de a atenua efectele rezistenței la antibiotice, oferind speranță în lupta continuă împotriva infecțiilor bacteriene.
Data publicării: 28 februarie 2025

